 사진=서울대서울대학교 의과대학 연구진이 폐암의 발병과 세포 노화 간의 연결고리를 결정짓는 핵심 조절 인자를 세계 최초로 밝혀냈다. 서울대 기초의학교실 이민재 교수팀은 25일, 폐선암(lung adenocarcinoma) 세포에서 세포 운명을 좌우하는 단백질 ‘UBR4’의 기능을 규명했다고 밝혔다. 이번 연구는 미국 국립과학원 회보(PNAS) 6월 18일자에 게재됐다.
사진=서울대서울대학교 의과대학 연구진이 폐암의 발병과 세포 노화 간의 연결고리를 결정짓는 핵심 조절 인자를 세계 최초로 밝혀냈다. 서울대 기초의학교실 이민재 교수팀은 25일, 폐선암(lung adenocarcinoma) 세포에서 세포 운명을 좌우하는 단백질 ‘UBR4’의 기능을 규명했다고 밝혔다. 이번 연구는 미국 국립과학원 회보(PNAS) 6월 18일자에 게재됐다.
폐선암은 전체 폐암의 약 40~50%를 차지하며, 치료가 어려운 대표적 난치성 암이다. 흡연, 대기오염 등 환경적 요인과 깊은 관련이 있지만, 그 발생을 유도하는 분자적 기전은 아직까지 명확히 밝혀지지 않았다.
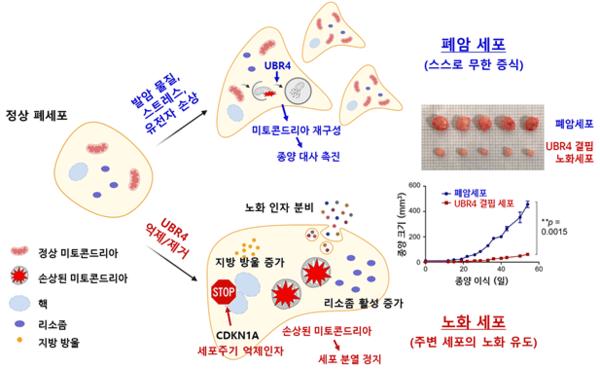
이 교수팀은 UBR4가 폐선암의 성장과 밀접한 관련이 있으며, 이 단백질이 존재하면 종양 대사가 활발해져 폐암이 발생하는 반면, 제거될 경우 세포는 암으로 가지 않고 노화 상태로 진입한다는 점을 동물 실험 및 환자 조직 분석을 통해 확인했다.
UBR4는 원래 세포 내 단백질을 분해하는 유비퀴틴 연결효소로 알려져 있었지만, 정확히 어떤 단백질을 대상으로 작용하는지, 또 어떤 생리·병리적 역할을 하는지는 미지의 영역으로 남아 있었다.
이번 연구에서는 특히, UBR4가 손상된 세포 내 미토콘드리아를 재조직하여 암세포의 활발한 에너지 생산과 증식을 도운다는 점이 규명됐다. 반대로 UBR4가 결핍되면 세포 내 오토파지(자가포식작용)가 비정상적으로 작동하며, 에너지 고갈, 산화 스트레스 증가, 리소좀 기능 저하 등의 연쇄적 반응을 일으켜 세포는 자연스럽게 노화 상태로 진입하게 된다. 더 나아가 이 노화된 세포들은 주변 세포에까지 노화 신호를 퍼뜨리는 것으로 확인됐다.
연구진은 폐선암 환자 샘플을 분석한 결과, 암이 진행될수록 UBR4 단백질의 발현량이 유의미하게 증가한다는 사실도 밝혀냈다. 마우스를 이용한 동물모델 실험에서도 UBR4를 제거하면 폐암세포의 성장이 사실상 차단됐다.
이민재 교수는 “UBR4는 암세포의 무한 증식을 유도할 수도, 반대로 세포를 노화 상태로 유도할 수도 있는 '세포 운명의 스위치'와 같은 존재”라며 “이번 연구는 암을 새로운 방식으로 제어할 수 있는 가능성을 보여준 첫 사례”라고 밝혔다.
이번 연구는 생화학 전공의 이민재·조성엽 교수, 병리학 전윤경·고재문 교수, 의과학 권용태 교수, 서울대병원 의생명연구원 한도현 교수 등 다학제 협업을 통해 진행됐다.
연구진은 향후 후속 연구를 통해 UBR4의 기능을 약물로 억제하거나 유전자 편집기술을 통해 폐암뿐 아니라, 미토콘드리아 기능 이상을 동반한 다양한 암에 적용할 수 있는 치료 전략으로 발전시킬 계획이다.
 바이씨즈, 실리프팅 브랜드 ‘자보실’로 리뉴얼… 볼륨실 ‘자보쇼츠’ 출시
메디컬 뷰티 테크기업 '바이씨즈'가 실리프팅 브랜드 ‘자보핏(ZAVOFIT)’을 ‘자보실(ZAVO THREAD)’로 리뉴얼하고, 특허받은 D-MESH(더블메시) 구조 기반의 차세대 볼륨실 ‘자보쇼츠(ZAVO SHORTS)’를 새롭게 선보였다. 이번 리브랜딩과 신제품 출시는 바이씨즈의 프리미엄 실리프팅 라인업을 한층 강화하는 계기가 될 것으..
바이씨즈, 실리프팅 브랜드 ‘자보실’로 리뉴얼… 볼륨실 ‘자보쇼츠’ 출시
메디컬 뷰티 테크기업 '바이씨즈'가 실리프팅 브랜드 ‘자보핏(ZAVOFIT)’을 ‘자보실(ZAVO THREAD)’로 리뉴얼하고, 특허받은 D-MESH(더블메시) 구조 기반의 차세대 볼륨실 ‘자보쇼츠(ZAVO SHORTS)’를 새롭게 선보였다. 이번 리브랜딩과 신제품 출시는 바이씨즈의 프리미엄 실리프팅 라인업을 한층 강화하는 계기가 될 것으..
 정덕영 클릭트 대표, 독자 기술인 XR 스트리밍 지연 보정 기술로 ‘대통령 표창’ 수상
클릭트는 정덕영 클릭트 대표가 산업통상자원부 국가기술표준원이 13일 주최한 ‘2023 신기술실용화 촉진대회’에서 ‘XR을 위한 화면 지연 보정을 위한 MTP Latency 개선기술’에 대한 높은 기술력과 뛰어난 공로로 기술개발과 제품화, 관련 산업기술진흥에 기여한 공을 인정받아 산업기술진흥유공 신기술실용화 부문 대통령 표창.
정덕영 클릭트 대표, 독자 기술인 XR 스트리밍 지연 보정 기술로 ‘대통령 표창’ 수상
클릭트는 정덕영 클릭트 대표가 산업통상자원부 국가기술표준원이 13일 주최한 ‘2023 신기술실용화 촉진대회’에서 ‘XR을 위한 화면 지연 보정을 위한 MTP Latency 개선기술’에 대한 높은 기술력과 뛰어난 공로로 기술개발과 제품화, 관련 산업기술진흥에 기여한 공을 인정받아 산업기술진흥유공 신기술실용화 부문 대통령 표창.
 푸마가 성사시킨 두 천재의 만남, 망누스 칼슨과 펩 과르디올라
글로벌 스포츠 기업 푸마(PUMA)가 맨체스터 시티 풋볼 클럽(Manchester City Football Club), 체스닷컴(Chess.com)과 함께 두 천재: 축구계의 펩 과르디올라(Pep Guardiola)와 체스계의 매그너스 칼슨(Magnus Carlsen)의 독점 대담을 론칭했다. 이 푸마 홍보대사들은 자신의 커리어에서 잊을 수 없는 순간에 대해 이야기하고, 두 스포츠의 전략과 전술을 자세히 들려...
푸마가 성사시킨 두 천재의 만남, 망누스 칼슨과 펩 과르디올라
글로벌 스포츠 기업 푸마(PUMA)가 맨체스터 시티 풋볼 클럽(Manchester City Football Club), 체스닷컴(Chess.com)과 함께 두 천재: 축구계의 펩 과르디올라(Pep Guardiola)와 체스계의 매그너스 칼슨(Magnus Carlsen)의 독점 대담을 론칭했다. 이 푸마 홍보대사들은 자신의 커리어에서 잊을 수 없는 순간에 대해 이야기하고, 두 스포츠의 전략과 전술을 자세히 들려...

